
伴随着科学研究的开疆扩土,脂肪移植已经由前期单一的体积填充扩展至干细胞疗法应用方面。科学家们追求将自体脂肪组织制备成各种“剂型”,以期最大化利用干细胞的功能,为病患带来效果更好、更稳定、系统的安全治疗方案。
近日,日本药企武田公司与比利时生物技术公司Tigenix联合宣布,其脂肪干细胞制剂——Cx601的3期临床达到了主要目标,能够显著改善克罗恩病患者肛瘘的愈合,并已在《The Lancet》期刊上正式公布了这项3期临床试验的成果。
但其实早在2012年1月,韩国食品药品监督管理局(以下简称KFDA)就已经批准关于干细胞药物Cuepistem 的生产审批许可,成为世界上首个获批的脂肪干细胞治疗剂,用于治疗复杂性克隆恩氏并发肛瘘。
Cupistem治疗克罗恩病并发症肛瘘优势明显
2012年1月,一向以严苛著称的韩国食品药品监督管理局(KFDA)正式批准Cuepistem用于治疗复杂性克隆恩氏并发肛瘘,这是KFDA批准上市的首个脂肪干细胞治疗药物。业内专家指出,KFDA对新药的评审标准非常严格。Cuepistem前后经过了5年的临床试验,最终通过了KFDA的审批。
自上市以来,Cuepistem的安全性与临床疗效进一步得到充分认证。数据显示,患者早期接受Cuepistem治疗,可延迟或甚至不需要进行复杂肛瘘治疗手术。Cupistem通过麻醉状态下缝合瘘管后,直接将细胞均匀注射到瘘管中,以达到治疗目的。Cuepistem也是干细胞治疗剂中最早纳入医疗保险赔偿金覆盖范围的。
来自Cuepistem研发公司Anterogen的数据显示,Cuepistem对于促进克罗恩病患者复杂肛瘘的愈合,有明显的治疗优势。
什么是克罗恩病&肛瘘?
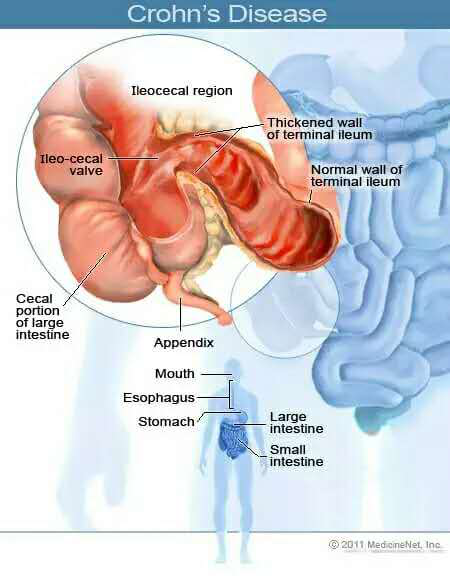
▲克罗恩病症状(图片来源:medicinenet.com)
克罗恩病(Crohn's disease)是一种慢性炎症性肠病,全世界发病人数在500万左右。克罗恩病患者要长期遭遇肠壁炎症,以及其他肠外表现,例如皮损、关节炎等并发症。其中,难以处理的,严重影响患者生活质量的并发症是复杂性肛瘘,往往久治不愈,缺乏有效的治疗手段。
肛瘘的发病率,国内统计为1.67%~2.6%,国外为8%~20%。发病年龄以20~40岁青壮年为主。以往的治疗手段主要以药物和手术治疗为主。这种传统的治疗方式虽然节省成本,但通常治标不治本,达不到完全根除疾病的治疗效果。
Cupistem是一种从自体脂肪组织提取的干细胞药物,来源广泛、取材容易、不涉及伦理问题、便于自体移植、无免疫排斥反应,利用脂肪干细胞的多能分化潜能,诱导分化成所需的组织,用以修补缺损促进伤口愈合,能使患者从根本上解决疾病困扰。
药物品质源于Anterogen公司的强大实力

干细胞药物Cupistem由Anterogen公司研发,而Anterogen是韩国最早进行干细胞技术研究的公司之一,掌握脂肪干细胞原创技术。
2007年,Anterogen公司成为拥有GMP级生产设施和质量规范的干细胞龙头企业之一,拥有获得最多许可的细胞治疗剂,进行干细胞治疗剂产品的开发及基础研究,实力引领韩国生命工程学技术。
干细胞药物Cupistem也在Anterogen公司的强大研发支持下,临床试验不断得到承认,最终获KFDA受批并远销海外。

GMP生产设施

Anterogen研究所

研发团队
此后5年里,Cuepistem不负众望,虽然临床治疗结果并未完全公开,但Cuepistem的研发公司Anterogen一直不断开发探索,现已技术出口到日本等地。

2009年,Cupistem克隆式瘘孔Ⅱ期临床试验得到承认;
2010年,Cupistem复杂肛瘘Ⅱ期临床试验也得到承认,并技术出口到日本;
2012年,Cupistem克隆式瘘孔Ⅲ期临床试验得到承认,KFDA正式批准Cuepistem的生产审批许可;
2013年,Cupistem克隆氏瘘治疗剂被正式开发应用;
2014年,Cupistem登状为保险赔付金,这也是最早可以申请保险赔付的干细胞药物。
Cuepistem或将迎来一场硬仗

Cuepistem背后不仅有实力雄厚的科研团队,更重要的是韩国KFDA及政府的政策监管。
KFDA成立于1996年,全称为韩国食品药品监督管理局,其职责是保障食品、药品等消费品的安全,以此来确保公民健康,并支持食品药品行业的发展。
2012年,KFDA批准Anterogen公司研发的关于肛瘘治疗药物Cuepistem的生产审批许可。同年,韩国政府就宣布将投入超过1000亿韩元以推动支持韩国在干细胞临床研究领域的发展,这些资金集中用于临床试验、干细胞治疗的安全性、干细胞研究的核心技术,以及干细胞领域相关人才的培养。
韩国政府还相应成立“国家干细胞银行”,以此进一步推动干细胞领域的生产、储存以及管理的标准化构建,另外,韩国成立了专门机构制定相关法律法规,组织专门人员进行严格审批,在行业内制定了完备指南。
然而,严格的药物审批制度和不完善的药物应用体系都将使其临床应用之路愈发难走。

目前,干细胞药物每次注射的费用都相当昂贵,(2011年上市的Cellgram-AMI药品每次注射费用相当于10万人民币)。这在一定程度影响了接受治疗的病人数。细胞治疗之所以价格不菲,主要由于生产成本很高。虽然现在Anterogen公司没有公布Cuepistem的临床治疗结果,但等待它的,或将是一场持久的硬仗。

每一个干细胞药物的问世都离不开国家政策的扶持和其研发团队的不断探索。即使前方还将面临重重考验,干细胞政策的颁布,医疗机构及企业的规范实施定会使干细胞全产业链更好地贯通。未来,上市的干细胞药物将会越来越多,并迅速受到大众的认可和消费。干细胞领域正在经历一场“渐行渐近”的革命,机遇已然来临。